“热力学的优点是它的高度可靠性与普遍性,……,热力学不能给出关于物质特性的具体知识,这是它的缺点。 [1]”“统计物理学正好弥补了热力学的这个缺点,解释了涨落现象。不但如此,统计物理学还可在对某种特殊物质作一些简单的物质的分子结构模型假设之后,推论出这种物质的特性。最重要的特殊物质的例子是理想气体。但统计物理学也有它的局限性。由于统计物理学中对物质的分子结构模型所作的简化假设只是实际的近似代表,所以理论的结果与实际不能完全符合。 [1]”
玻耳兹曼因子方法不仅与热力学基础知识一脉相承,而且巧妙地克服了“统计物理学处理互作用粒子系统所遇到的困难[2]”。由玻尔兹曼因子方法推导出来的描述实际气体的玻尔兹曼因子方程,不仅涵盖并超越了理想气体物态方程、范德瓦尔斯方程与维里方程[3],而且可以在理论上定量计算摩尔气体定压热容与定容热容之差;在实验测出定压热容的基础上,还可以在理论上定量计算出摩尔气体定压热容与定容热容之比。
1、理论计算公式的推导
由均匀物质的热力学关系式,可以求得定压比热与定容比热的差[1]
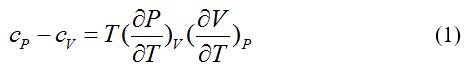
“这是一个很重要的公式, 表明两个比热的差可以应用物态方程求出[1]。”应用由玻耳兹曼因子方法推导出来的摩尔实际气体的玻尔兹曼因子方程[4]

并在压强 Pq,ΔPq,摩尔体积Vqm ± ΔVqm,温度 T± ΔT区间内,将摩尔表面自由能Fq 视为常量,即可得到
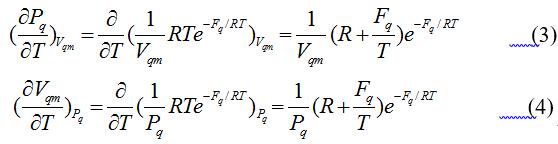
将式(3)与式(4) 代入式(1)可得摩尔实际气体的定压热容与定容热容的差
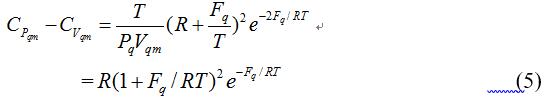
式(5)表明: 摩尔实际气体定压热容与定容热容之差是玻尔兹曼因子指数-Fq/RT 的函数,也可以说是分子相互作用特性Fq 的函数,是一个与分子平均间距(即摩尔体积)直接相关的物理量。
由于Fq 可以通过宏观物理量Pq ,Vqm , T,由式(2)计算出准确的数值,所以,应用式(5)可以在理论上定量计算出摩尔气体定压热容与定容热容之差。 如果已知CPqm (或CVqm )进一步还可以在理论上定量计算摩尔实际气体定压热容与定容热容之比
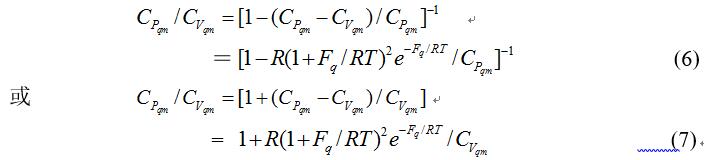
2、 摩尔理想气体的精确计算
如所熟知,理想气体状态下分子之间的平均间距r=∞,分子之间的相互作用力为零,故理想气体的摩尔表面自由能 Fq=0, e-Fq/RT=1,对于摩尔理想气体,式(5)与式(6)变为
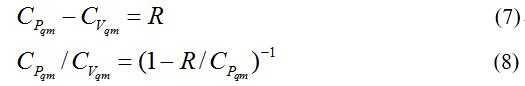
式(7)表明: 摩尔理想气体的定压热容与定容热容的差为 R,与理想气体物态方程 PqVqm = RT代入式(1) 的计算结果完全一致。
将25oC, 101。325kPa压强条件下的氢气近似视为理想气体,且Cp = 14268J/kg·K [5], 氢气的分子量为2.0157, R = 8.3128J/mol·K,代入式(8) 即可得到
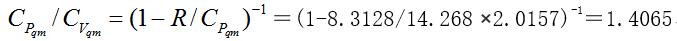
与氢气在0oC,101.325kPa条件下的实验观测(查表)值1.407[5]吻合得很好。
3、摩尔气体定压热容与定容热容之差、之比的理论计算
由式(5)与式(6)可以在理论上计算摩尔实际气体在不同环境条件下的定压热容与定容热容之差、之比。实例计算如表1、表2、表3所示。
表1 摩尔气体定压热容与定容热容之差、之比的理论计算[6]

结论:理论计算摩尔实际气体定压热容与定容热容之差、之比的结果,与实验观测值高度符合,证明公式(5)与公式(6)具有确切的实际应用价值与鲜明的基础理论创新意义。
表2 临界点上摩尔气体定压热容与定容热容之差的理论计算

推论: 临界点上摩尔气体定压热容与定容热容之差近似为常量0。65R,最大相对误差为2。1%。当然,这只是由公式(5)定量计算结果得出的推论。
表3 0oC,高压强条件下摩尔氢气定压热容与定容热容之差、之比的理论计算
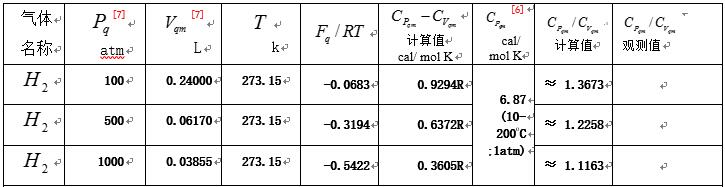
推论: 0oC条件下, 随着高压强的快速递增, 摩尔氢气定压热容与定容热容之差随之快速递减,趋向于0 ; 定压热容与定容热容之比随之快速地趋向于1。 当然,这只是由公式(5)与公式(6) 定量计算结果得出的推论。
4、 结论
1) 理论计算摩尔实际气体定压热容与定容热容之差、之比,与实验观测值高度符合的事实表明,公式(5)与公式(6)具有确切的实际应用价值与鲜明的基础理论创新意义。
2) 由公式(5)与公式(6)导出的两个推论顺理成章,期待能得到进一步的实验检验与验证。
参考文献:
[1] 王竹溪 2005。 热力学。 第2版。 (北京: 北京大学出版社。 ) 420~421, 94页。
[2] 汪志诚 2008 热力学 统计物理(第四版) 北京:高等教育出版社,265—270页
[3] 吴义彬 用玻尔兹曼因子方法精确计算分子相互作用特性 <<科学智慧火花>>栏目, 2015,08,27
[4] 吴义彬.实际气体的玻尔兹曼因子方程[J]。江西科学,2011,29(1),11页。
[5] [美]卡尔L,约斯,陶鹏万,黄建彬,朱大方(译)。MATHESON气体数据手册(第1版)[M]。北京:化学工业出版社,2003。432页。
[6] (苏联) К。П。雅阔夫列夫,黄镜权、尤烈之(译)。简明物理技术手册(第1卷)[M]。 北京:中国工业出版社,1966。 386页表2-29;458页表2-76.
[7] 钱尚武,章立源,李椿 热学(第2版)[M]。北京:高等教育出版社,2008。24页表1-3。