一、概述
基因工程(Genetic Engineering)是利用现代生物技术对生物体的遗传物质(DNA、RNA等)进行定向改造的一门科学。近年来,基因工程在基础研究、医疗、农业、工业及环境治理等领域取得了显著进展。
基因工程被称为基因拼接技术或 DNA 重组技术,是以分子遗传学为理论基石,借助分子生物学和微生物学的现代技术手段,将不同来源的基因按预先设计的蓝图,在体外构建杂种 DNA 分子,然后导入活细胞,以改变生物原有的遗传特性、获得新品种、生产新产品的遗传技术。
基因编辑是基因工程中的关键核心概念之一,它是指对生物体基因组特定目标基因进行修饰的一种基因工程技术。通过精确地删除、插入或替换基因组中的特定 DNA 片段,科学家能够实现对基因功能的调控,纠正遗传缺陷,甚至创造新的遗传特征。
重组 DNA 技术则是基因工程的核心操作技术,它通过将外源 DNA 片段与载体 DNA 分子连接,构建成重组 DNA 分子,然后将其导入宿主细胞中进行复制和表达。这一过程如同搭建积木,将不同的遗传元件组合在一起,创造出具有新功能的遗传物质。例如,将人类胰岛素基因与大肠杆菌的质粒载体连接,构建重组 DNA 分子,再导入大肠杆菌细胞中,大肠杆菌就能表达出人类胰岛素,用于治疗糖尿病。
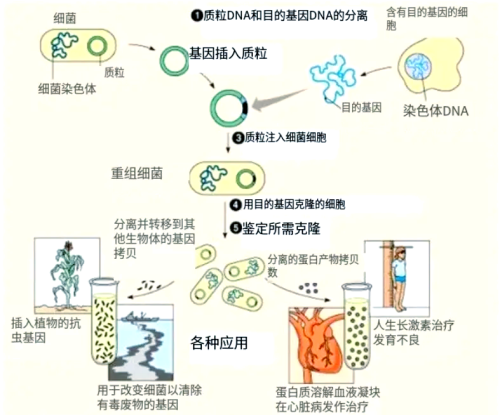
图片1:基因工程概述
二、基础研究进展
1.CRISPR-Cas9 基因编辑技术的优化
(1)CRISPR-Cas9 仍然是基因编辑的主流工具,近年来科学家开发了更高精度、更低脱靶效应的变体。CRISPR-Cas9 是一种革命性的基因编辑技术,源于细菌的天然免疫系统,现已发展成为精准修改生物体 DNA 的核心工具。其核心原理是模拟细菌抵御病毒入侵的机制,通过人工设计的“分子剪刀”实现对目标基因的定点编辑。
(2)Prime Editing (2019年)和 Base Editing (2016年),可实现单碱基编辑而不引起双链断裂。Prime Editing(先导编辑)是一种革命性的精准基因编辑技术,由David Liu团队于2019年首次开发。它突破了传统CRISPR技术依赖DNA双链断裂的限制,能够在多种生物系统中实现高精度、低脱靶的基因组修改
2.CRISPR-Cas12/Cas13 用于 RNA 编辑,拓宽了基因调控的范围。CRISPR-Cas12 与 CRISPR-Cas13 是两类功能截然不同的基因编辑与检测工具,其核心差异在于靶向分子(DNA 或 RNA)及附带切割活性("旁切效应"),在生物医学研究、精准诊断及治疗领域展现出革新潜力。
3.合成生物学的突破
(1)2023年,科学家在人工合成染色体方面取得重要进展。合成酵母基因组(Sc2.0计划) 已完成多个染色体的从头合成,为构建人工生命奠定基础。
(2)人体细胞智能化工程
① 可编程生物传感器:美国莱斯大学团队开发出新型蛋白质微处理器,在人体细胞内构建自定义信号响应线路,可实时监测炎症、癌症标志物或血糖异常,并在秒级时间内触发精准治疗反应,为慢性病管理提供新范式。
② 细胞兼容性优化:该技术能与细胞内天然过程并行运行,不影响正常功能,已成功抑制自身免疫性毒性。
(3)DNA/RNA操控技术升级
① 单链DNA规模化生产:新型催化型DNA技术(PECAN)实现任意序列单链DNA的克级量产,精确度达单碱基水平(纯度>98.5%),为基因编辑和材料科学提供基础元件。
② CRISPR多元化应用:基因编辑技术支撑合成生物学发展,2023年全球市场规模达66.2亿美元,推动精准基因改造效率提升5。
(4)生物材料创制革命
工程活体材料(ELM):通过改造枯草芽孢杆菌,在其表面展示硅矿化肽与自组装蛋白(SpyTag/SpyCatcher),成功合成力学性能增强的生物复合材料,实现材料可再生与功能定制。
4.DNA数据存储 技术发展迅速,微软等公司已成功在DNA中存储千兆字节的数据。DNA数据存储是一种利用生物分子特性保存数字信息的革命性技术,其核心是将二进制数据转换为DNA的碱基序列(A/T/C/G),再通过人工合成与测序实现数据的写入和读取。DNA存储以分子级的物质效率和跨时代的持久性,成为解决未来数据爆炸的关键技术方向。尽管产业化尚需突破成本与工程瓶颈,其潜力已重新定义了信息存储的终极形态
5.表观遗传编辑
科学家开发了 CRISPR-dCas9 结合表观修饰酶(如DNMT3A、TET1)的技术,实现在不改变DNA序列的情况下调控基因表达,应用于疾病治疗研究。
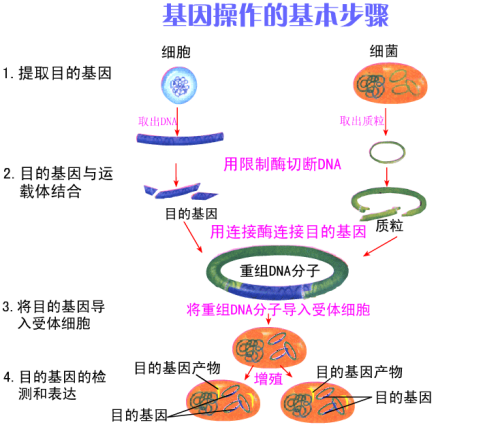
图片2:基因研究进展
三、医学应用突破
1.基因治疗
(1) FDA/EMA 批准的基因疗法 :
① Luxturna (2017,治疗遗传性视网膜病变)。Luxturna通过AAV载体基因置换修复RPE65功能,为特定遗传性视网膜病变患者提供了首个病因治疗手段,但高昂成本仍是普及挑战。其临床应用标志着基因治疗在眼科领域的重大突破,推动了中国等地的特许医疗政策落地。
② Zolgensma (2019,治疗脊髓性肌萎缩症SMA)。Zolgensma(通用名:onasemnogene abeparvovec)是全球首个获批用于治疗脊髓性肌萎缩症(SMA)的AAV基因治疗药物。
③ Casgevy (2023,全球首个CRISPR基因编辑疗法,治疗镰状细胞贫血和β-地中海贫血)。Casgevy是一种基于CRISPR/Cas9基因编辑技术的突破性疗法,用于治疗特定遗传性血液疾病。Casgevy代表了基因治疗领域的重大飞跃,但其普及仍面临技术复杂性与经济性挑战。随着生产流程优化及医保政策推进,未来有望惠及更多患者。
④ CAR-T细胞治疗 结合基因编辑技术,增强癌症免疫治疗效果。CAR-T细胞治疗是一种革命性的肿瘤免疫疗法,通过基因改造患者自身的T细胞来精准识别并消灭癌细胞。
⑤ mRNA 疫苗技术
mRNA疫苗技术是近年来生物医学领域的革命性突破,其核心原理是利用合成修饰的信使RNA(mRNA)指令人体细胞自主生成特定抗原蛋白,从而激活免疫应答。mRNA技术无需病原体培养、快速响应疫情、治疗场景多元。随着递送系统优化与临床适应症扩展,未来或将重塑疫苗开发与精准医疗的格局
⑥ COVID-19 大流行推动了 mRNA疫苗,该技术未来可能应用于癌症疫苗和传染病预防。COVID-19大流行作为全球公共卫生危机,直接加速了mRNA疫苗技术从实验室走向大规模应用的进程。这一变革推动WHO将mRNA技术纳入全球大流行防范核心战略,并为癌症、遗传病等治疗领域推开新大门。
⑦ 罕见病与遗传病治疗。从病毒载体到mRNA技术,遗传病治疗正经历从“延缓病症”到“根治病因”的范式转变。随着递送系统精准化与生产规模化,未来十年有望实现500+单基因遗传病的基因修正疗法覆盖,重塑罕见病治疗格局。
⑧ 2023年,科学家利用碱基编辑技术 成功在动物模型中修复了泰-萨克斯病(Tay-Sachs) 的致病突变。萨克斯病(Tay-Sachs Disease,TSD)是一种由HEXA基因突变引起的常染色体隐性遗传性溶酶体贮积症,导致β-己糖胺酶A(Hex A)功能缺失,引发GM2神经节苷脂在神经细胞内异常积累,造成进行性神经元损伤。萨克斯病作为罕见神经退行性疾病,当前治疗以延缓症状为主,但基因疗法的成功案例为根治带来曙光。

图片3:基因医学发展
四、农业与食品科学
1.基因编辑作物
CRISPR编辑作物 如抗褐变蘑菇、高番茄红素番茄、抗旱小麦等已进入市场或田间试验。CRISPR基因编辑技术在作物改良领域的应用正深刻改变现代农业格局,其核心突破在于精确、高效、低成本的基因组定点修饰能力。随着全球逾200种CRISPR编辑作物进入田间试验(截至2025年),这项技术有望成为保障粮食安全、应对气候危机的核心科技支柱
2.中国批准抗虫耐除草剂基因编辑大豆 (2022),美国批准 基因编辑高油酸大豆 (2023)。
(1)基因编辑技术推动抗虫耐除草剂大豆从“外源基因依赖”转向“内源精准优化”,在增产降本、减少农药依赖方面展现变革潜力。随着中国产业化试点扩大及南美新品种迭代,兼具高产与可持续特性的基因编辑大豆有望重塑全球大豆供应链,成为保障粮食安全的核心技术支柱。
(2)基因编辑技术推动抗虫耐除草剂大豆从“外源基因依赖”转向“内源精准优化”,在增产降本、减少农药依赖方面展现变革潜力。随着中国产业化试点扩大及南美新品种迭代,兼具高产与可持续特性的基因编辑大豆有望重塑全球大豆供应链,成为保障粮食安全的核心技术支柱。
3.畜牧业基因改良
通过基因编辑培育 抗非洲猪瘟猪 、低甲烷排放牛 等,提高养殖效率和环保性。畜牧业基因改良技术正通过基因编辑、智能化育种与政策支持实现跨越式发展。基因改良技术正从单一抗病育种向优质高产、资源节约、生态友好多维目标演进,政策与科技双轮驱动下,畜牧业产能与可持续性将同步跃升
4.细胞培养肉(人造肉)
(1)2019年南京农业大学周光宏团队培育出国内首块动物干细胞人造肉。
(2)2023年联合国FAO/WHO发布《细胞食品的食品安全问题》,建立全球监管框架。
(3)中国《“十四五”生物经济发展规划》明确支持细胞培养肉技术研发。

图片4:农业与食品科学
五、工业与环境应用
1.微生物工厂
微生物工厂是将微生物细胞改造为高效生物合成平台的技术体系,通过基因编程实现物质定向生产。利用合成生物学改造微生物生产 生物燃料(如异丁醇) 、塑料降解酶 和 高价值化合物(如青蒿素)。微生物工厂正重塑工业制造范式——以可再生的生物质替代化石原料,以细胞“绿色智造”推动碳中和目标,其核心价值在于用生物多样性解决资源有限性。
2.环境修复
基因工程微生物用于降解塑料(PETase/MHETase 酶) 和吸收重金属污染 。

图片5:工业与环境应用
六、中国基因工程科研进展及成果(近五年来部分)
1.2024年7月:中国科学院动物研究所李伟、周琪团队开发全RNA介导的基因精准写入技术(R2逆转座子工具),首次在多种哺乳动物细胞实现大片段基因(最高效率>60%)定点整合,突破传统DNA模板的免疫原性限制,为遗传病根治提供新路径。这项突破性成果,实现了人体细胞中精准的靶向基因整合,为基因组工程领域带来了前所未有的进展。
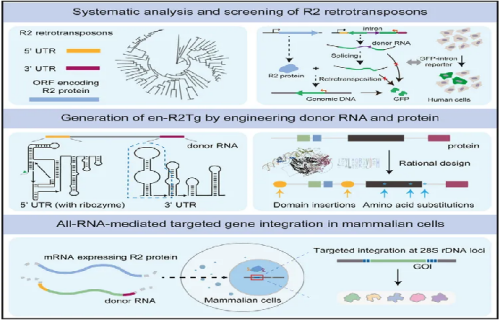
图片6:新型基因疗法
2.中国科学院遗传发育所高彩霞团队开发新型碱基编辑系统,CRISPR技术优化,实现单碱基到超大片段DNA的精准操纵,脱靶率控制在[7][9<0.001%,显著提升作物基因编辑安全性]。
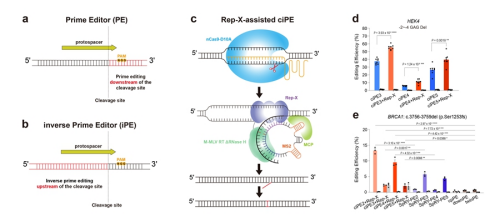
图片7:开发人类细胞中的反向引导编辑系统
3.中国科学院遗传发育所高彩霞团队高彩霞团队通过编辑水稻合成通路,创制全球首种能将Q9转化为人体必需Q10的稻米,兼具抗氧化与心血管保护功能。
4.中国科学院遗传与发育生物学研究所谢旗研究员团队开发可减少30%化肥使用的工程菌剂,提升作物氮利用效率;培育耐盐碱作物新品种(如谢旗团队解析耐盐碱机制)。
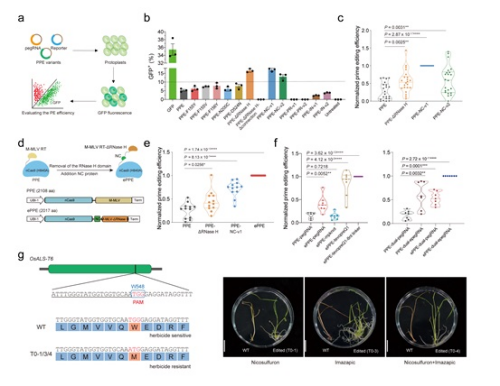
图片8:植物高效新型引导编辑器ePPE的建立及应用
5.中国农业科学院黄三文团队利用蔬菜基因组图谱,设计培育抗病高产番茄。
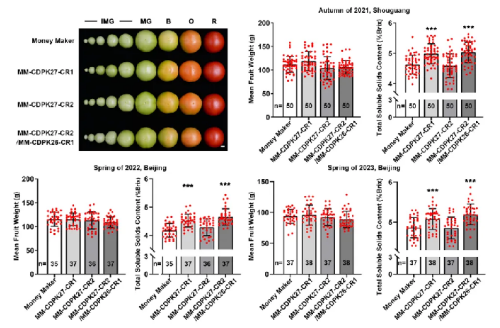
图片9:CDPK27 和 CDPK26 抑制糖分积累
6.中国农业科学院深圳农业基因组研究所(岭南现代农业科学与技术广东省实验室深圳分中心)萧玉涛团队在《细胞报告(Cell Reports)》上在线发表了题为“Landscape of structural variants reveals insights for local adaptations in the Asian corn borer”的研究论文。该研究通过构建首个亚洲玉米螟图形泛基因组(v1.0)、群体转录组、QTL定位等方法,揭示了基因组的结构变异(SVs)在适应性进化中的作用。
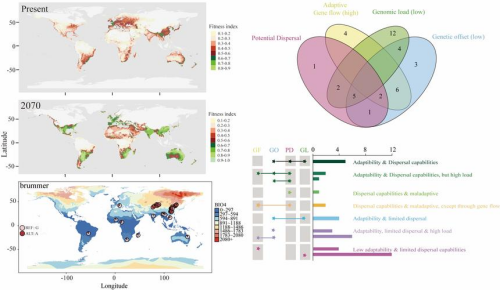
图片10:棉铃虫响应气候变化的适应性演化机制
7.西湖大学(中国科学院参与合作)高晓飞团队基于rbcDNA多癌种检测模型,实现1-2ml血液同步筛查7类癌症(灵敏度93%-96%),成本降至传统技术1/106。
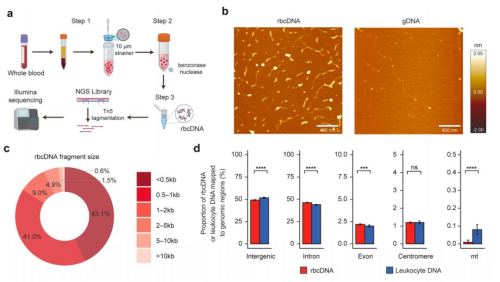
图片11:高精度癌症早期检测的潜力
8.华为"深瞳"AI系统模拟癌症突变,辅助个体化治疗方案制定。
9.北京大学团队开发化学重编程技术,皮肤细胞转干细胞效率提升至90%,推动个性化细胞治疗落地。

图片12:邓宏魁教授(右一)在指导学生做实验
10.中国科学院动物所刘光慧团队揭示人类基因组暗物质驱动衰老机制,绘制全球首张红细胞残留DNA(rbcDNA)图谱,阐明癌细胞远程操控机制。
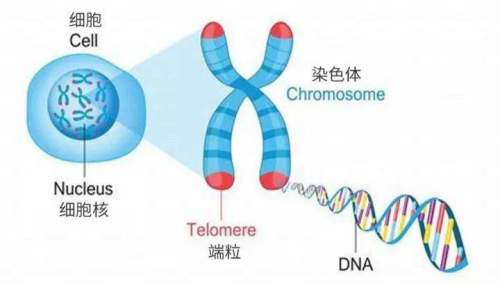
图片13:细胞核内端粒的长度是衡量细胞衰老的重要标志
11.2025年5月中国科学院昆明动物所联合东南亚机构完成东南亚人群基因组图谱,系统揭示该区域人群遗传结构,填补全球基因组"南方盲区"。
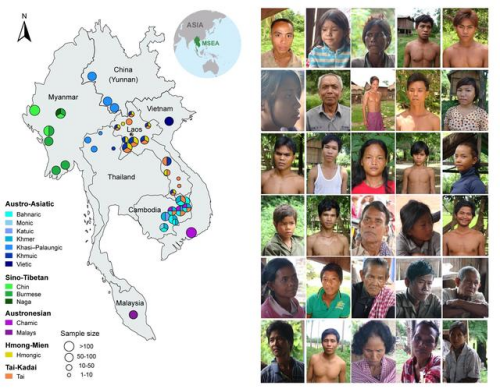
图片14:东南亚基因组计划一期SEA3K的人群分布和组成
12.中科曙光建成生物信息计算平台,支撑基因组数据自主分析。
13.天枢系统于2022年5月在厦航集团主用上线,自此成为国内首个通过局方审定并投入主用的、自主研发的支持洲际运行的全功能国产计算机飞行计划系统。天枢系统实现了飞行计划可视化、运算速率跨方位提升等,大大增强了系统使用的高效性和准确性。"天枢计划"构建国家生物样本库,突破国际数据封锁。
七、未来展望
1.精准医疗 :精准医疗是一种基于个体基因、环境及生活方式差异,制定个性化疾病预防与诊疗方案的现代医学范式。其核心目标是实现“医源性损害最小化、医疗耗费最低化及病患获益最大化”。
(1)个体化基因疗法
个体化基因疗法是基于患者的特定基因突变或生物标志物,定制针对性的基因治疗策略,以实现精准医疗的目标。近年来,基因编辑技术(如CRISPR)、载体优化和生物信息学的进步推动了个体化基因疗法的快速发展。精准医疗正从“对症用药”迈向“对人下药”,其核心价值在于以生物多样性解决健康需求的有限性。
(2)癌症早筛与治疗
早筛的核心是"高危人群精准筛查+预警信号及时响应"。肺癌、消化道癌、乳腺癌可通过现有手段早期发现,而泛癌种血液检测技术或将在未来5年改变筛查模式。确诊后需根据分期选择手术、靶向或免疫治疗,晚期患者亦可从ADC药物等新疗法中获益。未来核心方向在于融合多组学数据建立个体化风险地图,真正实现“早筛五年,生机翻倍”。
2.农业可持续发展 :气候适应性作物、氮高效利用作物。农业可持续发展需兼顾技术革新(有机肥/智慧农业)、制度设计(土地流转/生态补偿)与利益共享(农民增收/三产融合)。
3.生物计算与存储 :生物计算与存储正推动“硅-碳融合”范式变革,DNA存储将在文化遗产、医疗大数据领域率先商用,而类器官计算或重塑AI芯片产业格局,DNA存储技术可能成为未来大数据解决方案。
4.合成生命 :人工合成基因组推动“设计生命”研究。人工合成基因组技术正在从根本上重塑生命科学领域,通过编程生物系统实现“设计生命”的目标,在医学、工业和环保领域展现出变革性潜力。合成生物学正推动“生命2.0革命”,模块化基因元件库(如BioBrick)支持生命体构建,而人类基因组合成计划或将在10-20年内重塑医学与农业范式。
结论
基因工程正在深刻改变医学、农业、工业和环境科学,但也面临伦理、安全和监管挑战。随着技术不断优化,未来有望解决更多全球性问题,如疾病治疗、粮食安全和环境污染等。
参考文献
1.中国政府官网
2.中国科技部官网
3.国家自然科学基金委官网
4.中国科学院科研进展官网
5.中国工业信息化产业部官网
6.中国卫健委官方网站
7.中国医科院官方网站
8.中国医学科学院北京协和医学院医药生物技术研究所
9.中国科学院微生物研究所官网
10.中国生物工程学会官网
11.中国轻工业联合会官网
12.中国生物发酵产业协会官网
13.中国生物发酵工程协会官网
14.中国生物技术信息官网
15.中国农业科学院微生物研究所官网
16.中国数子科技馆官网
17.中国遗传学会官网
18.中国生物医学工程学会官网
19.乌日斯哈拉 基因工程技术在农业生产中的应用成果 农业工程技术 . 2024 ,44 (10)
20.李哲 转基因技术在我国生物制药领域的应用与发展 中国医药技术经济与管理 . 2008 (06)
21.中创网 我国在医药生物技术领域取得系列重大成果 中国药科大学学报 . 2002 (06)
22.孟小雄 基因工程技术的新成果——抗虫植物 植物杂志 . 1986 (06)
23.马若轩 浅谈基因工程对遗传病治疗作用 现代医学与健康研究电子杂志 . 2017 ,1 (08)
24.彭瑶 井冈霉素高产菌株的基因工程改造 上海交通大学上海市211工程院校
25.孙春杰 高产纳他霉素基因工程菌株的构建 天津科技大学 硕士电子期刊 2019年第04期
26.陈章良 基因工程——跨越生物种的遗传物质“拼接技术” 知识就是力量 . 2015 (09)
27.张小华 姚庆 收秦加 阳刘秀 珍王越嗣 医学院校基因工程教学实践探索 西北医学教育 . 2013 ,21 (06)