一、基因工程概述
基因工程(又称基因拼接技术或DNA重组技术)是指按照人类意愿,在生物体外对遗传物质进行设计、改造,并通过特定技术导入受体细胞,从而定向改变生物遗传特性的技术。
基因工程是以分子遗传学为理论基础,以分子生物学和微生物学的现代方法为手段,将不同来源的基因按预先设计的蓝图,在体外构建杂种DNA分子,然后导入活细胞,以改变生物原有的遗传特性、获得新品种、生产新产品的遗传技术。基因工程技术为基因的结构和功能的研究提供了有力的手段。
基因工程是生物工程的一个重要分支,它和细胞工程、酶工程、蛋白质工程和微生物工程共同组成了生物工程。它是用人为的方法将所需要的某一供体生物的遗传物质——DNA大分子提取出来,在离体条件下用适当的工具酶进行切割后,把它与作为载体的DNA分子连接起来,然后与载体一起导入某一更易生长、繁殖的受体细胞中,以让外源物质在其中“安家落户”,进行正常的复制和表达,从而获得新物种的一种崭新技术。
图片1:基因工程概念
二、基因工程的本质
1.物质操作层面
本质是对DNA分子的定向改造,通过人工剪切、拼接、重组不同来源的DNA片段,实现对生物遗传特性的精确调控。
2.遗传学原理层面
核心是基因重组,即在分子水平将外源目的基因与载体结合,跨物种转移并表达,形成新的遗传组合。此过程不创造新基因,而是重组自然界已有基因资源。
3.技术特征层面
属于人工干预的DNA重组技术,需依赖工具酶(如限制性内切酶、连接酶)、载体系统(如质粒)及宿主细胞表达体系,实现遗传信息的定向编辑与功能优化。
三、基因工程原理
1.原理
基于基因重组。在生物体进行有性生殖过程中,控制不同性状的基因发生重新组合的现象,它是生物变异和进化的重要来源之一。
2.关键工具
(1)"分子手术刀"限制性核酸内切酶(精准切割DNA)。是一类由原核生物(主要是细菌)产生的、能特异性识别双链DNA中的特定核苷酸序列并在特定位点切割磷酸二酯键的核酸内切酶。
(2)"分子缝合针":DNA连接酶(连接DNA片段)。是生物体内关键的酶类,主要负责催化DNA链中相邻核苷酸间磷酸二酯键的形成,实现DNA片段的连接。
图片2:基因工程工具
(3)载体:将重组DNA导入宿主细胞的运输工具(如质粒、病毒)。
① 质粒是存在于细菌、酵母等微生物细胞中,独立于染色体外的环状双链 DNA 分子(少数为 RNA 或线性结构),具有自主复制能力。
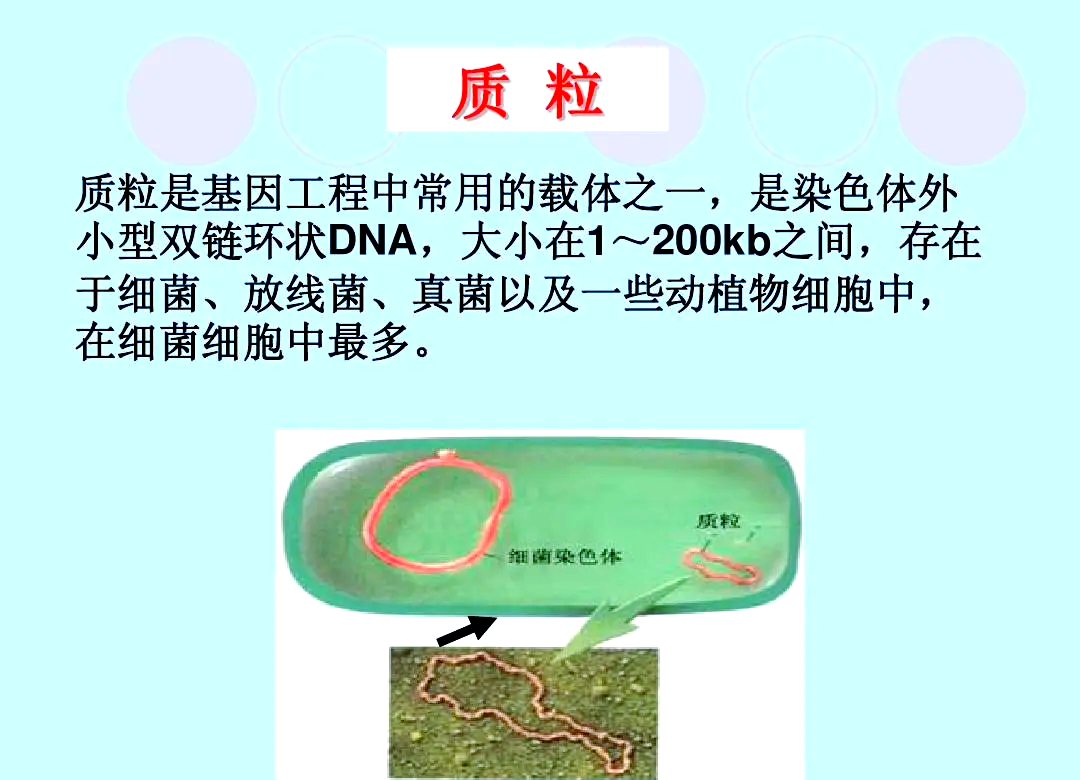
图片3:质粒概念
② 病毒是一种非细胞生命形态,它由一个核酸长链和蛋白质外壳构成,病毒没有自己的代谢机构,没有酶系统。因此病毒离开了宿主细胞,就成了没有任何生命活动、也不能独立自我繁殖的化学物质。
四、基因工程技术理论三大发现
1.发现了遗传物质——DNA
1944年,艾弗里(O.T.Avery)的肺炎双球菌转化实验。美国细菌学家艾弗里在格里菲斯实验的基础上,通过体外实验继续探究“转化因子”的化学本质。通过分离和提纯,艾弗里从加热杀死的S型菌中提取出了蛋白质、DNA和多糖等物质。他将这些物质分别加入R型活菌的培养基中,结果发现,只有加入DNA,R型活菌才能转化成S型活菌。基于这一结果,艾弗里认为,DNA是携带遗传信息的物质。
2.揭示了遗传物质的分子机制:DNA分子的双螺旋结构和半保留复制。1952年,奥地利裔美国生物化学家查伽夫(E.chargaff,1905-2002)测定了DNA中4种碱基的含量,发现其中腺嘌呤与胸腺嘧啶的数量相等,鸟嘌呤与胞嘧啶的数量相等。这使沃森、克里克立即想到4种碱基之间存在着两两对应的关系,形成了腺嘌呤与胸腺嘧啶配对、鸟嘌呤与胞嘧啶配对的概念。1953年,沃森(J.D.Watson)和克里克(F.Crick)了DNA双螺旋结构模型、半保留复制图,获1958年诺贝尔奖。
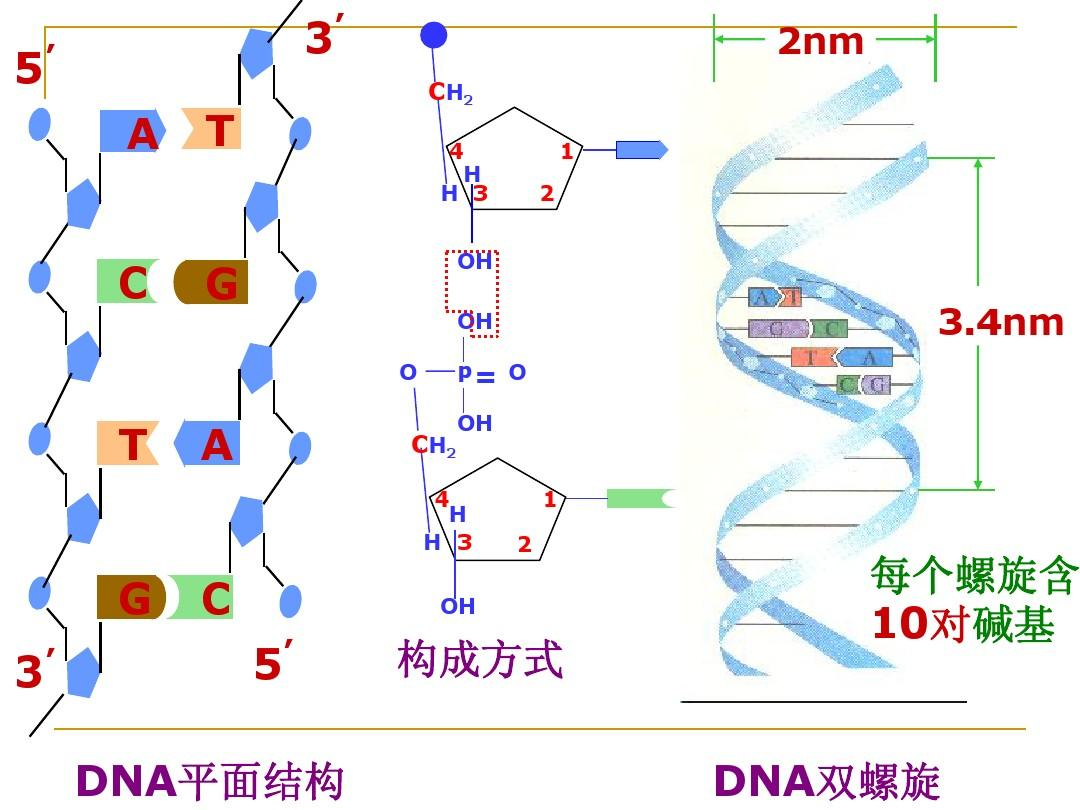
图片4:DNA分子的双螺旋结构
3.确立了遗传信息的传递方式:以密码形式传递
1963年,美国尼伦伯格(M.W.Nirenberg)和马太(H.Matthaei)确立了遗传信息以密码形式传递,破译了编码氨基酸的遗传密码(3个核苷酸=1个密码子=1个aa)。
五、基因工程技术三大突破
1.世界上第一个重组DNA实验:实现不同来源DNA的体外重组。1972年斯坦福大学化学家伯格(P.Berg)借助内切酶和连接酶将猴病毒SV40的DNA和大肠杆菌λ噬菌体的DNA在试管中连接在了一起,第一次成功地实现了DNA的体外重组。
图片5:基因重组
2.第一个基因克隆实验:重组DNA表达实验,是世界上第一个基因工程实验。1973年美国斯坦福大学医学院遗传学家科恩(S.Cohen)将体外构建的含有四环素和卡那霉素抗性基因的重组质粒导入大肠杆菌,获得了具有双抗性的大肠杆菌转化子,成功完成了第一个基因克隆实验,是基因工程诞生的标志。
3.第一个真核基因在原核生物中的表达:第一次实现了异源真核基因在原核生物中的表达。1974年,科恩(S.Cohen)和博耶(H.Boyer)将非洲爪蟾编码核糖体基因的DNA片断同pSC101质粒重组,并导入大肠杆菌细胞,结果表明动物基因已进入大肠杆菌并转录出相应的mRNA产物,第一次实现了异源真核基因在原核生物中的表达。
六、基因工程技术操作原理
(一)目的基因的获取
(1)基因文库筛选法。从基因组文库或cDNA文库中筛选含有特定基因的DNA片段。
① 基因组文库是将某种生物的全部基因组DNA切割成长度适宜的片段,并与载体连接后导入宿主细胞群体所形成的克隆集合,是保存和研究生物遗传信息的核心工具。
② cDNA文库是指将特定生物个体、组织或细胞在某一发育阶段表达的全部mRNA经逆转录形成的互补DNA(cDNA)片段,与载体连接后导入宿主细胞形成的克隆集合。
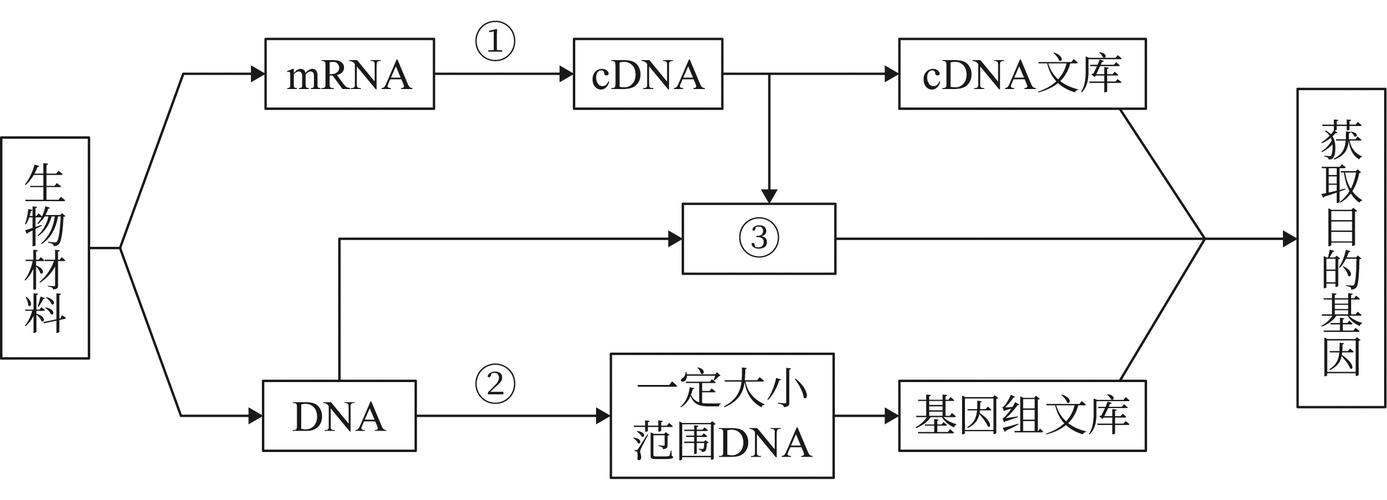
图片6:目的基因的获取
(2)PCR扩增技术技术原理与步骤:PCR扩增技术(聚合酶链式反应)是一种在体外对特定DNA片段进行指数级扩增的分子生物学核心技术。
① 基本机制:
第一、变性(温度95℃):
作用:使双链DNA解离为单链模板。
关键:时间需充分(通常30秒–3分钟),GC含量高或模板复杂时需延长变性时间或提高温度。
PCR(聚合酶链式反应)中的变性步骤是通过高温破坏DNA双链间的氢键,使其解离为单链模板的过程。
第二、退火(温度55–60℃):
作用:引物与单链DNA模板特异性结合。
关键:温度需优化,计算公式:Tm = 4(G+C) + 2(A+T),实际退火温度比引物最低Tm值低3–5°C56。时间通常为30–60秒。
退火是PCR反应中继变性后的关键步骤,指温度降低至特定范围(通常50-65℃),使引物通过碱基互补原则结合到单链DNA模板的两端,形成局部双链结构,为后续延伸阶段提供起点。
第三、延伸(温度72℃):
作用:DNA聚合酶沿模板合成新链。
关键:延伸时间按扩增片段长度设定,一般 1kb/min(如1kb片段需1分钟,>4kb需延长至3–4分钟)。
PCR(聚合酶链式反应)中的延伸步骤是指在退火后,DNA聚合酶以单链DNA为模板、在引物引导下合成新DNA链的关键阶段。
第四、循环25–30次后,目标DNA可扩增百万倍。PCR循环是聚合酶链式反应(PCR)的核心过程,通过重复的温度变化实现DNA的指数扩增。
②核心组分:
第一、模板DNA:需控制量与纯度(如人基因组DNA推荐30–100 ng)。在PCR(聚合酶链式反应)中,模板DNA是扩增目标片段的起点和基础,其质量、浓度和来源直接影响反应效率和结果的可靠性。
第二、引物:设计决定扩增特异性与片段长度。PCR引物是人工合成的寡核苷酸序列,需与目标DNA区域两端的模板链互补配对,作为DNA聚合酶启动合成新链的起点。在PCR中,引物特异性结合模板DNA,引导DNA聚合酶沿模板延伸合成新链,实现目标片段的指数扩增。
第三、耐热DNA聚合酶:Taq酶(耐95℃高温)是关键,无需每轮循环补充酶,实现PCR自动化,推动自动化扩增。
催化DNA合成:在72℃延伸温度下高效合成DNA新链,扩增速率可达2000碱基/分钟
第四、dNTPs与缓冲液:提供原料及适宜反应环境。
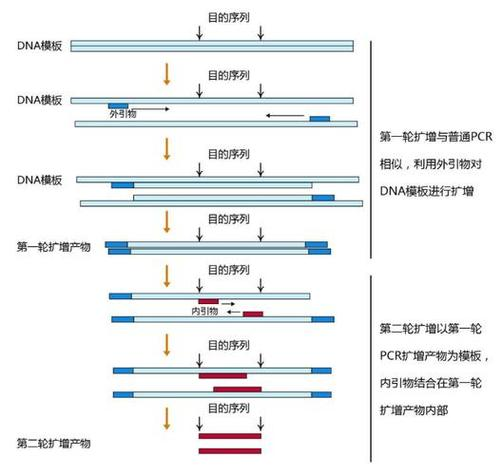
图片7:利用两套pcr引物进行两轮pcr扩增 第二轮的扩增产物才是目的基因片段
(3)人工合成法
针对已知序列的小分子基因,直接通过DNA合成仪化学合成。人工合成法是通过化学或酶促手段直接合成目的基因片段,无需依赖生物体天然DNA模板。
(二)基因表达载体的构建
1.载体组成
包含目的基因、启动子(驱动转录)、终止子、标记基因(用于后续筛选)。
2.重组操作
用同种限制酶切割目的基因和载体,形成匹配末端,再通过DNA连接酶连接重组。
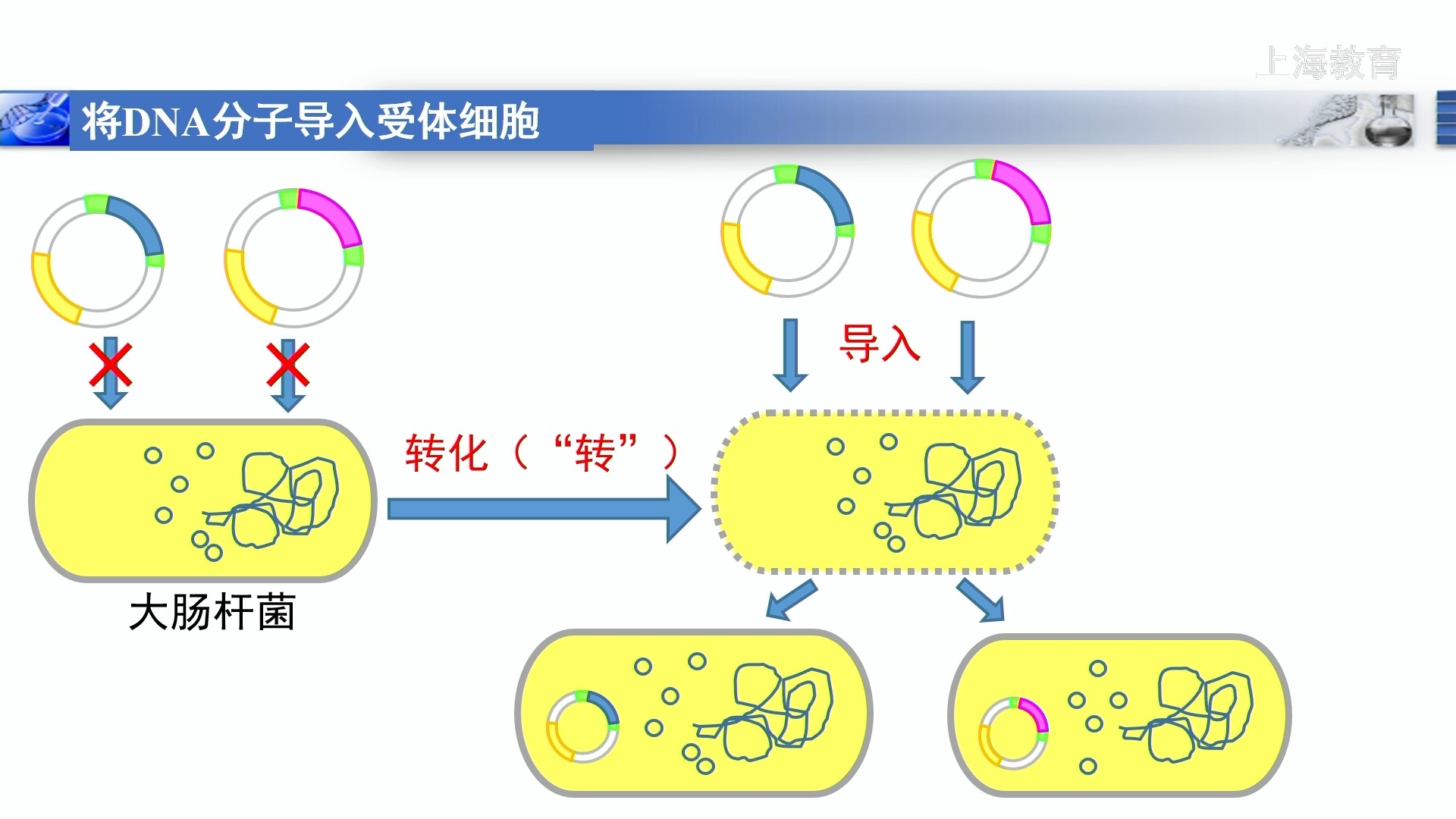
(三)目的基因导入受体细胞
1.植物细胞
(1)常用农杆菌转化法或基因枪法。
①农杆菌转化法是一种利用根癌农杆菌(Agrobacterium tumefaciens)的天然基因转移能力,将外源DNA导入植物细胞的关键生物技术。
②基因枪法是一种通过物理方式将外源基因导入细胞的转基因技术,其核心原理是利用高速金属微粒携带外源DNA穿透细胞壁/膜,实现基因转移。
2.动物细胞
多采用显微注射技术(如受精卵受体)。显微注射技术是在高倍倒置显微镜下,通过显微操作器控制玻璃微量注射针,对细胞或早期胚胎。进行精密操作的方法。其核心原理是将外源物质(如精子、DNA、细胞器)直接注入目标细胞内,实现基因编辑、辅助受精或细胞功能研究。
3.微生物细胞
如大肠杆菌:用Ca²⁺处理制备感受态细胞,热激促进重组DNA导入。
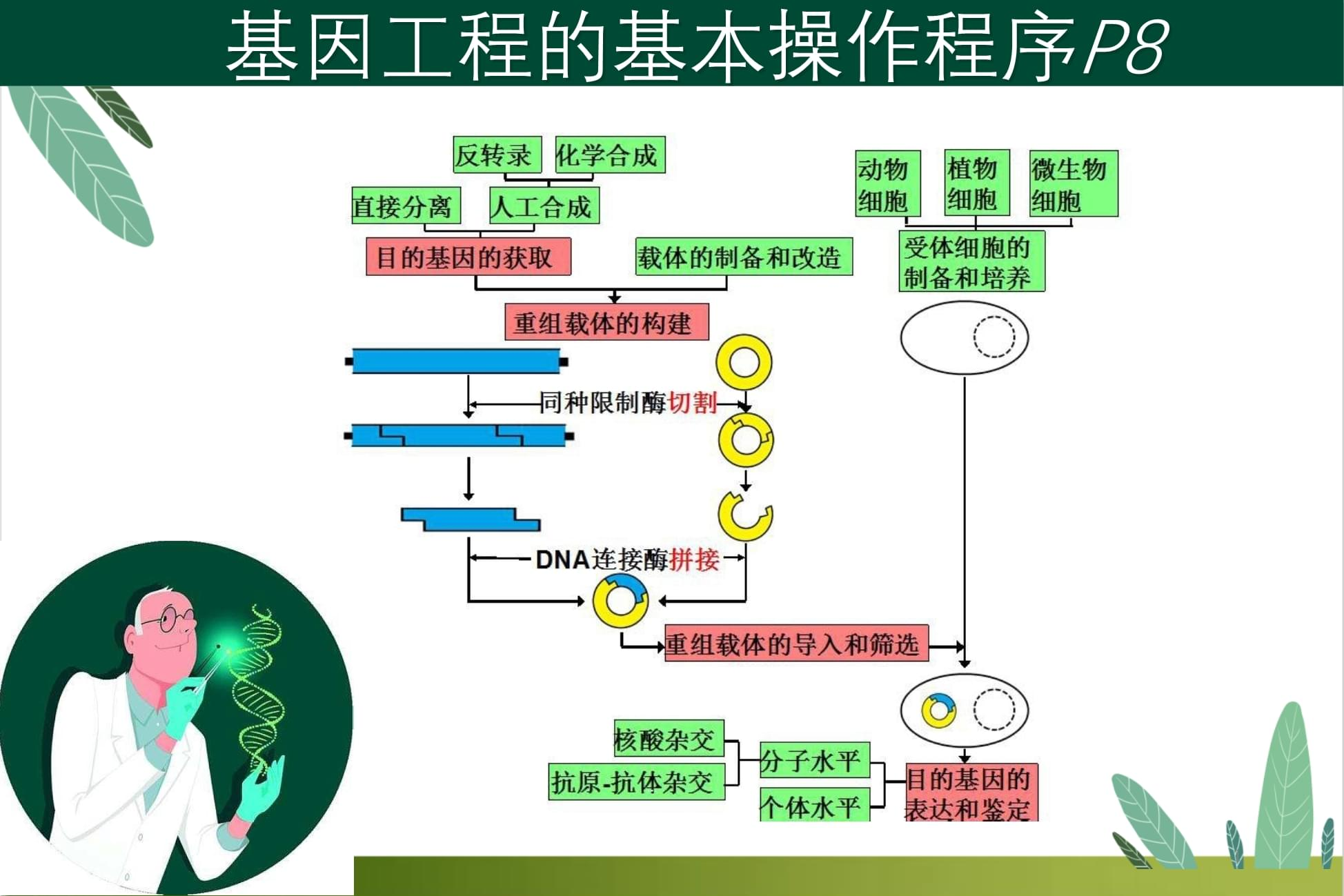
图片8:基因构建
(四)目的基因的检测与鉴定
1.DNA水平检测
用DNA分子杂交技术确认染色体是否整合目的基因。
2.转录水平检测
通过核酸杂交检测mRNA是否生成。
3.翻译水平检测
提取蛋白质进行抗原-抗体杂交或功能活性验证。
4.表型筛选
利用标记基因(如抗生素抗性)筛选成功转化的受体细胞。
5.应用实例
胰岛素生产:将人胰岛素基因导入大肠杆菌,通过发酵大规模生产胰岛素,显著降低糖尿病治疗成本并提升安全性。
6.说明:流程需严格无菌操作,涉及PCR仪、离心机、电泳设备等工具510;标记基因(如抗性基因)是筛选重组体的关键。
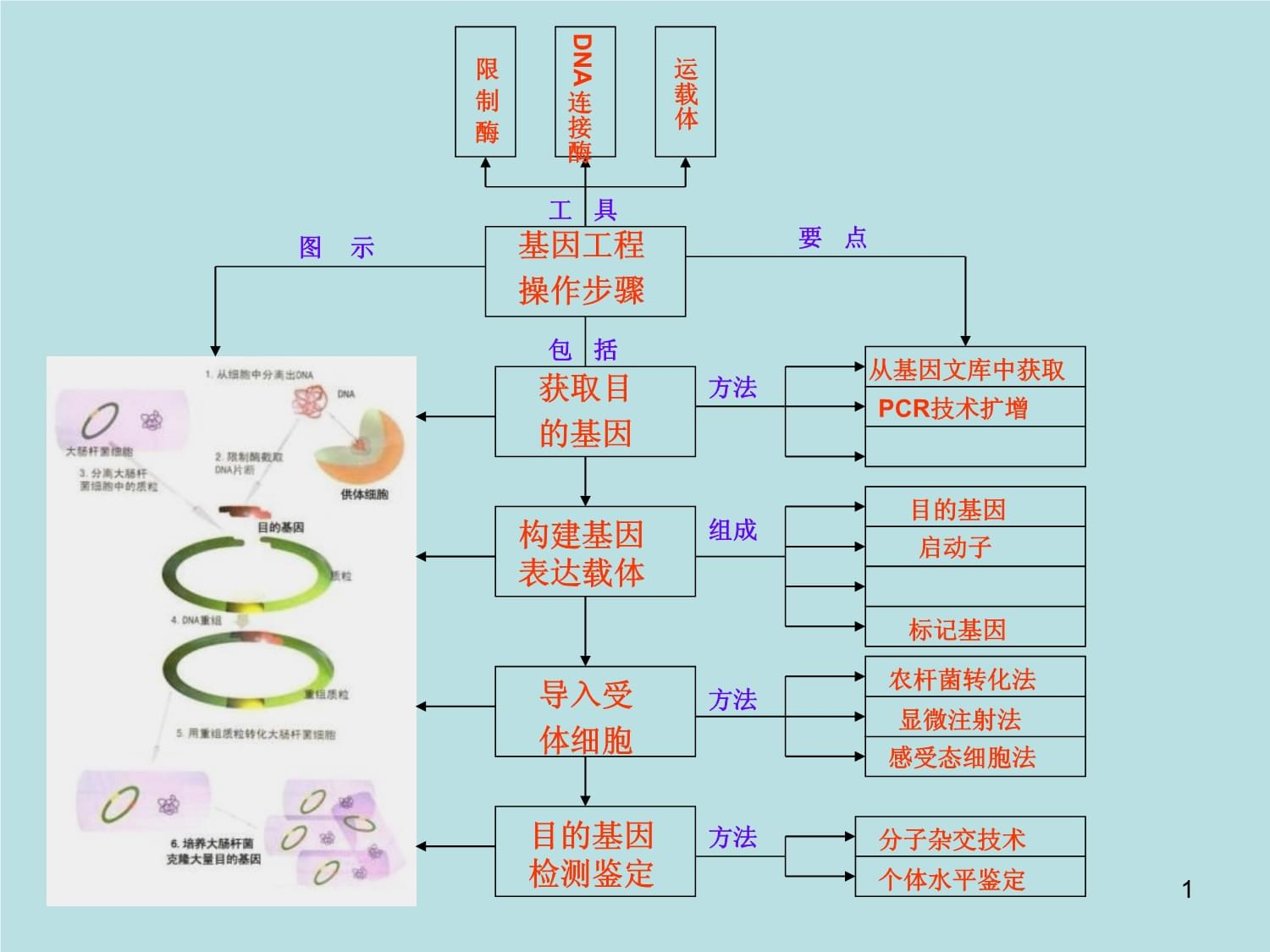
图片9:基因工程操作步骤
七、发展前景
基因工程在农业、医药、工业等领域有着广泛的应用前景。例如,通过基因工程技术可以培育出抗虫、抗病、高产的作物新品种;可以生产出具有治疗作用的基因药物;还可以利用微生物发酵生产有价值的化合物。随着CRISPR/Cas9等新型基因编辑技术的出现和发展,基因工程将更加高效、精确和安全地服务于人类社会的发展。
参考文献
1.中国政府官网
2.中国科技部官网
3.国家自然科学基金委官网
4.中国科学院科研进展官网
5.中国工业信息化产业部官网
6.中国科学院微生物研究所官网
7.中国生物工程学会官网
8.中国轻工业联合会官网
9.中国生物发酵产业协会官网
10.中国生物发酵工程协会官网
11.中国生物技术信息官网
12.中国农业科学院微生物研究所官网
13.中国数子科技馆官网
14.中国遗传学会官网
15.中国生物医学工程学会官网
16.张恬嘉 微生物代谢途径的基因工程改造及应用研究 工业微生物 . 2025 ,55 (01)
17. 杨冬 生命编程:基因工程的奇迹与挑战 百科知识 . 2024 (32)
18.蒋道梅姚 新欣 杨琴 张鹏 TP53基因工程抗体的构建、表达筛选及表征鉴定 赣南医学院学报 . 2024 ,44 (06)
19.曾凡洪 基因工程中PCR技术常考知识点的归纳与拓展 中学教学参考 . 2024 (14)
20.范丽娟 佟辉 创新混合式教学在生物化学重组DNA技术(基因工程)教学中的应用 生命的化学 . 2023 ,43 (11)
21.徐笑宇 董陈文 华字淑 慧刘涛 李建宾 基因工程原理与技术课程建设和教改探索 大学教育 . 2023 (22)
22.刘伟杰 基于材料基因工程技术的Fe-Co-Ni基γ'相强化型高熵合金的设计及性能研究 桂林电子科技大学 2024-05-16
23.祝晓莉 孙超 李春华 徐臣善 多基因共表达载体构建的研究进展 山东林业科技 . 2023 ,53 (02)
24.盛文龙 郑重 例析PCR技术在基因工程中的应用 教学考试 . 2023 (15)
25.范桂枝 杨海昕 曾凡锁 齐凤慧 詹亚光“基因工程原理与技术”课程思政教学调研和设计 教育教学论坛 . 2022 (07)
26.王沁芸 潘晔 陈克平 王慧英 吕鹏 基因工程抗体及其在识别小分子中的应用 生物学杂志 . 2021 ,38 (02)