一、 抑郁症是一场全球健康危机
如今,被称作“黑狗”的抑郁症已经成为了一场全球健康危机。根据WHO在2020年的统计数据,全球有3亿抑郁症患者(WHO, 2020);而中国流行病调查显示抑郁症患病率为3.4%(Huang et al., 2019);中国每年因抑郁症造成的经济损失高达494亿元(WHO, 2017)。
抑郁症是最常见、全年龄段疾病负担最重的精神疾病,还有着自杀的严重后果。面对如此庞大的抑郁症群体,然而目前在医学上缺少客观的生物学指标对抑郁症进行诊断,也就是说我们不能像诊断肺炎那样,通过验血或是对身体某个部位的扫描就可以对抑郁症进行精准的诊断和分型。这是因为不同于病毒感染或炎症反应等生理病变,抑郁症的改变藏匿于人类十分特殊的大脑功能之中,人脑约占人体总重量的2%,但即使不执行任何特定的认知任务,它消耗的能量约占身体产生总能量的20%,这些与认知、人格、疾病和意识相关的内在活动十分复杂。不过,最新的一些认知神经科学研究已经开始尝试初步读取“抑郁的大脑想什么”,并期待为抑郁症的诊疗提供一些更为客观的参考。
二、 抑郁症的表现及其发病机制
1、抑郁症的表现
抑郁症的表现具有多样性和差异性,很多患者的症状有相同之处,也有不同之处,这也给抑郁症的诊断带来了一些困难。有的患者存在早醒的睡眠问题,有自杀的意念,食欲也不好;有的患者表现为认知障碍,如注意力无法集中;有的患者精神兴奋或迟滞,有抑郁情绪,或者非常疲劳,做所有的事情都没有快乐的感觉。请警惕以上工作生活中的种种表现,因为它们都有可能是抑郁症的具体症状。
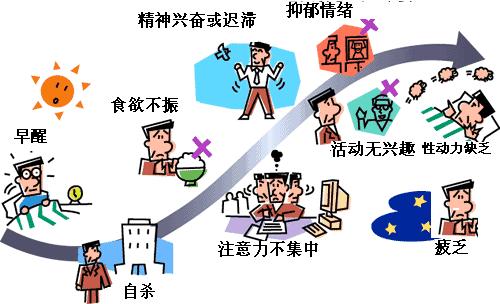
图1:抑郁症的临床表现
目前,精神科医生就是通过问询患者有哪些临床表现来对抑郁症进行诊断的。专业的医生会考虑患者是否在连续两周的时间内,在如下症状中表现五项以上症状(前两项核心症状至少含有一项),从而确定患者是否真的患上了抑郁症。
l情绪低落、心境抑郁
l兴趣减退、愉悦感丧失
l体重显著减少或增加
l失眠或者睡眠过多
l精神运动激越或迟滞
l感到疲劳,缺乏精力
l感到自己没有价值,或者自罪自贬
l注意力和思考能力下降或犹豫不决
l自杀念头、自杀计划或自杀行为
2、抑郁症病因的复杂性
抑郁症的病因到现在依然不是那么清楚,我们不能准确的说出一个人为什么患上了抑郁症。现代科学发现导致抑郁症的可能因素有很多,包括遗传因素、神经生物学因素和心理社会因素,而这几种因素通常会共同存在于一位抑郁症患者身上并且相互作用。
(1)遗传因素
其中抑郁症的遗传度大概有30%~40%左右,并没有达到双向情感障碍和精神分裂症那么高,但对抑郁症的发病依然具有影响。例如在家系研究中,著名作家海明威的家族就有一个“自杀魔咒”:海明威的父亲、妹妹、兄弟、孙女和他自己全部死于自杀。这就像是一个中了“魔咒”的“自杀家族”,而追问其科学原因,很可能是海明威的家族中含有了抑郁症的高发基因。
(2)神经生物学因素
关于病因的神经生物学因素,神经科学研究主要关注大脑中神经递质的异常和脑网络的异常,这两个层面的抑郁的神经机制我们会在下文详细介绍。
(3)心理社会因素
抑郁发病的心理社会因素也不容忽视,例如负性生活事件、早期童年经历、生活状况和社会支持等因素都可能和抑郁症有关。例如,我们团队感兴趣早期不良抚育导致抑郁样行为的神经基础(Yan et al.,2017)。就是说如果小时候受到了虐待或者童年成长环境不好,会对大脑产生了什么影响呢?
我们就对于大鼠进行了研究。动物研究的一个优势是实验者可以对大鼠进行操纵。我们让大鼠在童年期有一些受虐的行为,童年期受虐组(Maltreated)大鼠会在成年期表现出比正常组(Control)大鼠更多的抑郁样行为,包括在糖水偏好测试(Sucrose preference test)里不爱喝糖水了,在强迫游泳测试(Forced swim test)里会很快地放弃,在社交测试(Social interaction test)里面,就像人类抑郁症患者一样有很多的社交退缩行为。
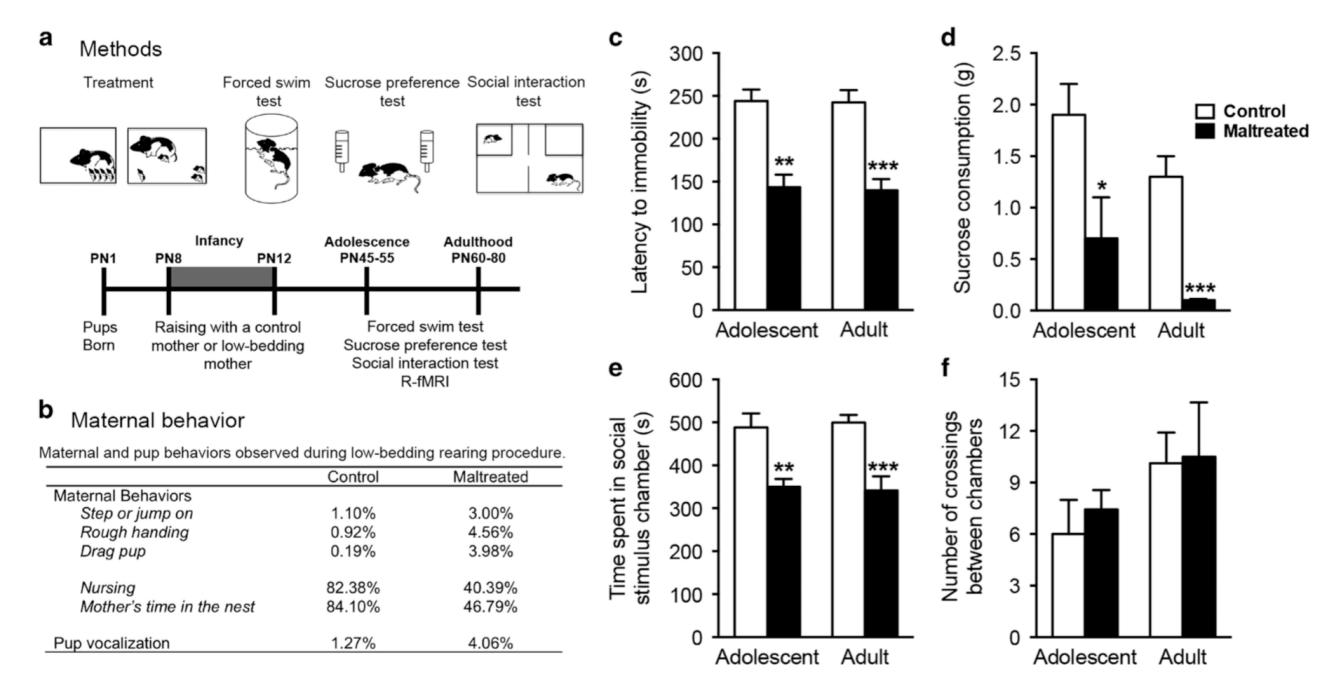
图2: 大鼠不良抚育导致抑郁样行为研究
(4)抑郁症的复杂性
值得注意的是,患上抑郁症的人可能存在较大的个体差异,例如不是所有的抑郁症患者都经历过重大的负性生活事件。所以,作为“精神”疾病的抑郁症的病因是相对复杂的,不像一般的“身体”疾病的病因那样明确。例如就在2019年底首次爆发的新冠肺炎的病因已经十分明确,在生物学上被发现为感染了一种新型的冠状病毒,而了解了新冠肺炎的病因就可以很好地对该疾病筛查诊断和对症用药。所以,目前有很多的科学研究同样聚焦于在生物学水平上寻找抑郁症的病因,试图进而寻找治疗抑郁症的“特效药”。
一、 抑郁的大脑与正常的大脑存在不同吗?
1、神经元释放神经递质异常
那么抑郁症患者大脑中的神经递质有什么异常呢?现在一个非常流行的假说是神经递质假说(monoamine theory)。
为了搞清楚神经递质假说,我们先来了解一下大脑中神经细胞的工作过程。我们知道大脑中神经信号的传递是通过神经元完成的。那么两个相连的神经元,前一个神经元的电信号要传递到后一个神经元,具体是怎么传递过去的呢?
如图3所示,前后两个神经元连接的地方叫突触间隙。前一个神经元胞体里面含有很多的囊泡,囊泡里面存储着很多的神经递质(neurotransmitter)。神经电信号来到后,前一个神经元就会把内部的囊泡运到表面,然后把里面的神经递质释放到突触间隙的位置。接着后一个神经元表面有一些受体(receptor),这些受体接收神经递质,然后产生新的神经电信号,再往下一个神经元继续传递。
这是神经元之间正常的传递过程。而在神经递质假说中,抑郁症患者存在着神经递质的异常,常见的如五羟色胺神经递质的异常。即抑郁症患者神经元释放到突触间隙中的五羟色胺神经递质是少于正常水平的,突触间隙中神经递质浓度降低,就会导致神经信号传递的减弱。而后一个神经元长期接受不到足够多的神经递质,就会在表面长出更多的受体去试图接受更多的神经递质。然而,由于突触间隙中本身神经递质的浓度较低,神经信号还是无法正常的传递。
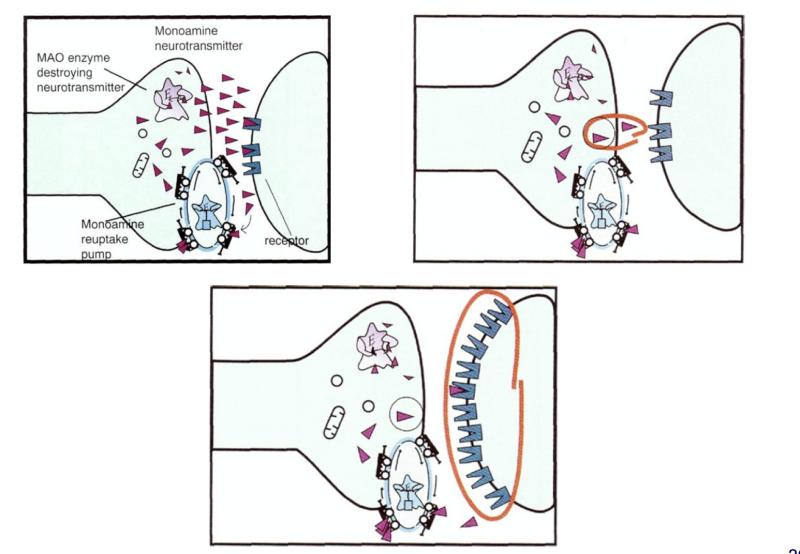
图3:抑郁症患者神经递质释放减少,导致神经元受体增多
这就是基于大脑神经元水平的一种抑郁症假说,它的直接证据是有一类抗抑郁药物是通过神经递质起作用的,后文我们会进一步地介绍药物是怎么通过影响神经递质的传递来改善抑郁的。
2、脑网络不同
人的大脑网络中包括一个称作默认网络(default mode network, DMN)的脑网络,它无时无刻不在运转,是大脑中消耗能量最多的网络。我们在说话,在做计算,甚至运动的时候大脑都会消耗很多的能量,其中很大一部分能量都由默认网络消耗。它跟我们的回忆过去,关注当下,计划未来都存在紧密的关系。默认网络分为三个子系统,有负责自我的核心子系统(DMN core),负责过去的内侧颞叶子系统(DMN MTL),和负责现在的背内侧前额叶子系统(DMN DMPFC),我们特别关注它,是因为它跟抑郁症患者的思维方式紧密相关。
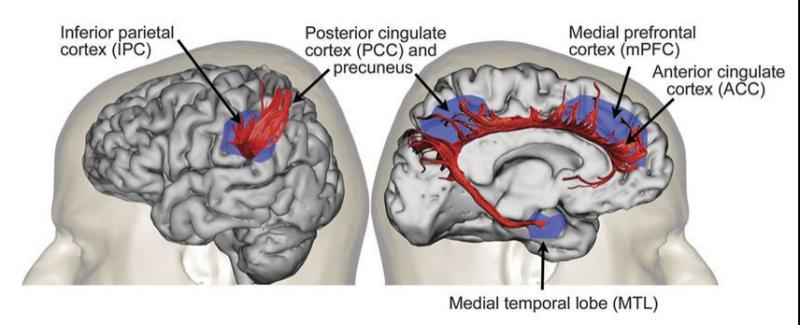
图4:大脑默认网络
我们在看似什么都不做的时候(即静息态,resting-state,指清醒但不进行任何特定任务的状态),我们的大脑依然在想很多很多的东西,心理学上称之为自发思维(self-generated thoughts)。研究发现,偏抑郁的人的自发思维内容中包括比正常人更多的反刍和反省(Li et al.,2022)。反刍思维(rumination)是对过去的悲伤事件本身及其后果和原因的反复咀嚼(Nolen-Hoeksema et al., 2008),它具有自我强化、循环往复、持续时间久的特点。比如抑郁症患者就会经常想:“为什么这种事情偏偏发生在我身上?”,“为什么总是我这么倒霉?”。然后自己也明明知道不要这样想,别人也告诉他不要想那些不好的东西,多想一些开心的事情。但是患者的大脑陷入了一种循环里面,在反刍思维中无法自拔。反刍思维能够预测抑郁症的发生和持续时间,即使是健康个体,反刍思维越多,越有可能罹患抑郁。此外,反刍思维还能够预测重性抑郁障碍患者的抑郁复发。

反刍思维有没有存在具体的脑生理机制呢?抑郁症患者(MDD)和正常人(NC)相比,他们大脑的默认网络存在功能连接(functional connectivity,FC)的减低,这可能是让他们陷入到抑郁的反刍思维中的原因(Yan et al.,2019)。对于功能连接减低,我们可以理解为大脑的不同脑区之前会组成一个通信网络,而功能连接可以反应这个网络的通讯效率,我们发现抑症患者的大脑网络通信效率要比健康人更低一些,可能导致他们的认知加工速度变慢。
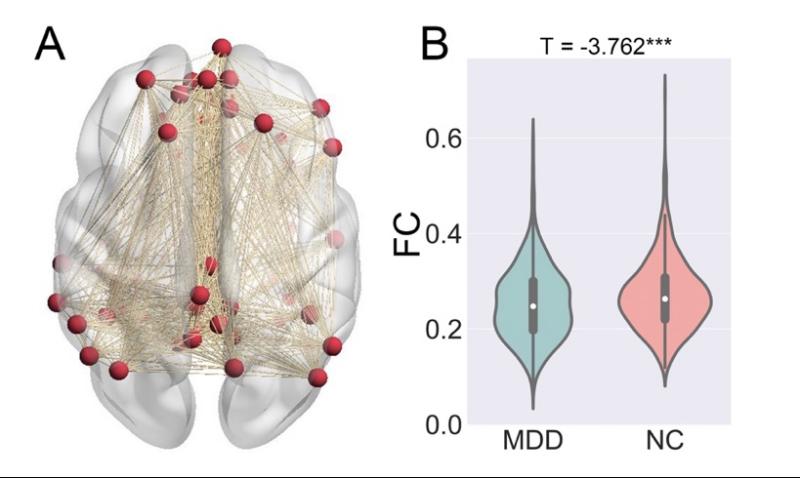
图6:患者大脑默认网络功能连接减低
而根据我们开发的反刍思维的任务态范式,实验发现反刍的时候我们的想法更加的负性,更加的悲伤,更加的关注过去,更加的关注自我,是一种言语性思维,这是反刍的思维特点(Chen et al., 2020)。

图7:反刍思维任务态范式,包括静息态、悲伤回忆、反刍、分心(参照条件)等阶段
但是我们更感兴趣的是反刍思维的脑神经机制,它是如何让我们的大脑陷在里面不能自拔?我们发现在反刍的时候,在默认网络中负责自我的核心子系统跟负责过去的内侧颞叶子系统交互非常的紧密,表示沉溺在过去之中;而跟负责现在的背内侧前额叶子系统功能连接的降低,表示不能充分的关注当下。由此我们实验室可以提供一些假说,由于关注自我的核心子系统跟关注现在的背内侧前额叶子系统功能连接降低,不能充分的关注当下,所以人会陷入抑郁反刍的痛苦里面。(Zhou, …, Yan*, 2020; Chen, …, Yan*, 2020)。
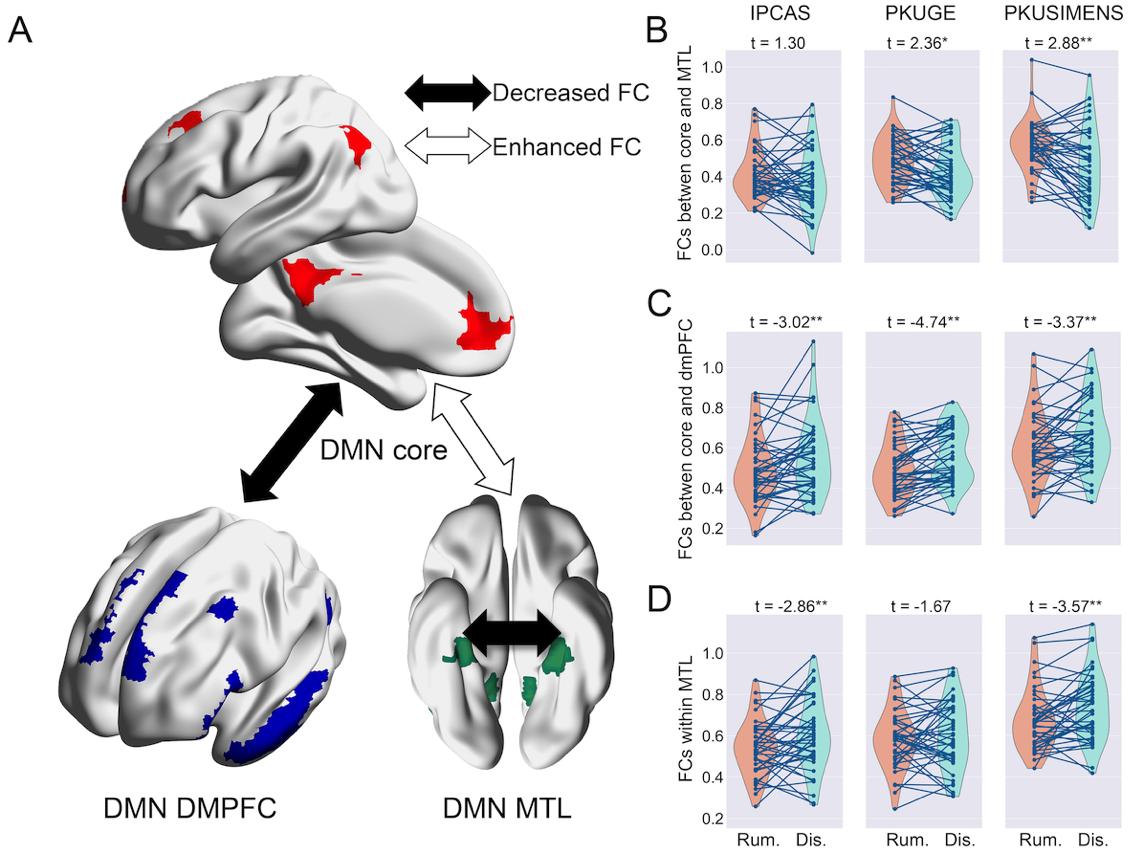
图8:反刍思维期间,默认网络核心区域(DMN core)与默认网络内侧颞叶(DMN MTL)子系统间的功能连接增强,而默认网络核心区域与默认网络背内侧前额叶皮层(DMN DMPFC)子系统间的功能连接减弱
四、脑科学研究在抑郁症诊治中的应用
在抑郁症的诸多病因中,即使是心理社会学因素,也一定有其神经生物学的基础。而利用大脑静息态功能性磁共振成像(resting-state functional magnetic resonance imaging,R-fMRI)等方法不仅适用于研究与静息态的“抑郁”大脑紧密相关的反刍思维等的心理机制,还能够获得相应的神经生物学指标作为一种更为客观的医学指标(目前抑郁症的临床诊断和治疗中所缺乏)。下面介绍的应用研究便着重关注抑郁症的脑神经基础,研究者们试图更加精准地确定抑郁症的生物学标记,从而更好地服务于抑郁症的分型诊断和对症治疗。抑郁症常见有心理治疗、药物治疗和物理治疗等方法。
1、心理治疗
现在西方非常流行的正念疗法,常常要求练习者进行冥想,深呼吸,关注当下,不做评判……这也是源于我国传统佛学文化的一种治疗方式。既然抑郁症患者的反刍思维具有沉溺过去,不能充分关注当下的特点,那么正念治疗的恰恰可以改善这一点。例如在中国科学院心理研究所的正念生活小组中,我们可以练习感受自己的每一次呼吸,练习感受行走和进食的过程……练习感受当下的发生的一切。
那么正念疗法究竟对抑郁症患者的大脑造成了什么影响?正念是否可以加强默认网络核心子系统与背内侧前额叶子系统的功能连接,降低默认网络核心子系统与内侧颞叶子系统间的功能连接,从而降低我们的抑郁?研究结果恰恰显示,正念冥想可能对改变大脑的功能连接和反刍思维这种负性的思维方式起到作用(Shen et al., 2020)。
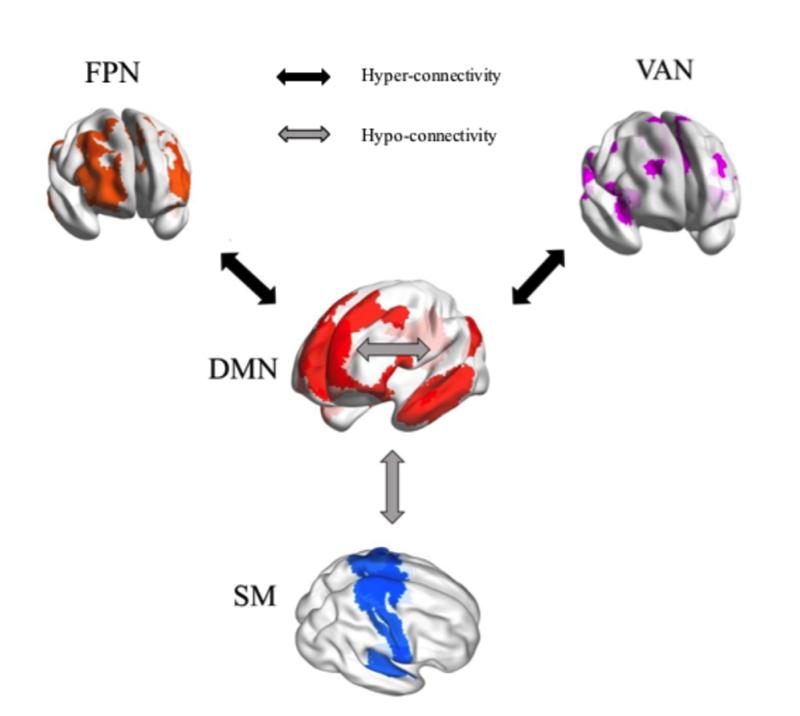
图9:冥想期间,默认网络(DMN)内部功能连接减弱,默认网络与躯体运动网络(SM)功能连接减弱,默认网络与额顶控制网络(FPN)和腹侧注意网络(VAN)功能连接增强
2、药物治疗
在药物治疗方面,现在有很多种类的药物都可以治疗抑郁。如果患者的抑郁到了一定严重程度,医生就会建议患者服用抗抑郁药物。其中有大约1/3的患者非常的幸运,服用第一种药物就会有效果,还有大约1/3的患者就需要调换不同的药物,另外其余大约1/3的患者药物对他们是不起作用的,我们后面会讲这些患者可能需要采取其他治疗手段。
(1)传统抗抑郁药物SSRI
那么药物究竟是怎么对患者的大脑起效的呢?现在最流行的一类治疗抑郁症的药物叫作五羟色胺再提取抑制剂(SSRI),其包括西酞普兰、氟西汀、舍曲林、帕罗西汀等。这些药物就参与了神经递质传递的过程。
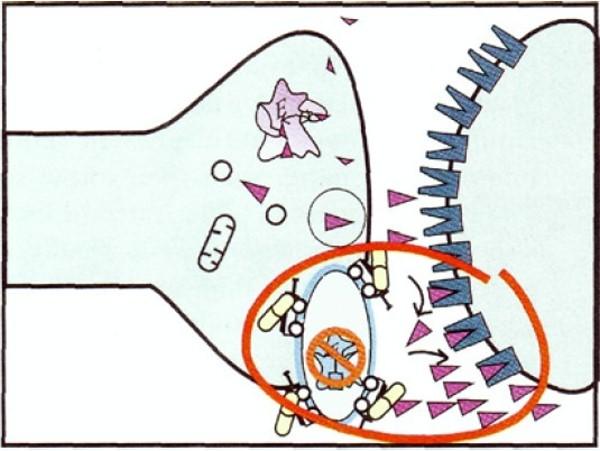
图10: 回收机制被阻断
我们上文提及的神经递质假说中,抑郁症患者神经元突触间隙中的神经递质是低于正常水平的。而正常神经元中的信号传递是神经递质从前一个神经元的囊泡中吐出来到突触间隙中,再被后一个神经元表面的受体接收,最后神经递质又会被前一个神经元的转运体(位于图10圆圈处)回收以准备下一次的神经信号释放。
那么SSRI正是通过阻断这个回收机制起作用的。一旦前一个神经元的转运体停止回收神经递质,突触间隙中的神经递质就会增多,等浓度回到正常水平之后,后一个神经元表面多长出来的受体便会降低到原本的数量。所以SSRI就是通过调节大脑神经递质的回收机制来改善抑郁的。而这种药物的起效周期一般比较长,当神经递质浓度的降低被抑制之后,多长出来的受体需要慢慢的消减下去。所以在抑郁症的治疗中,一定要认真听医生的话,坚持服药才能产生疗效。
在大脑网络层面,抗抑郁药物又会对大脑的功能连接带来什么改变?我们实验召集了一组抑郁症患者连续服用抗抑郁药物八周,并在吃药前后分别扫描了大脑的静息态数据,发现脑网络的功能连接会出现明显的降低,这个降低跟抗抑郁药物的疗效有关系,药物会阻断五羟色胺转运体,然后保持突出间隙的神经递质浓度,进而降低大脑静息态的功能连接改善抑郁(Li, et al., 2021)。
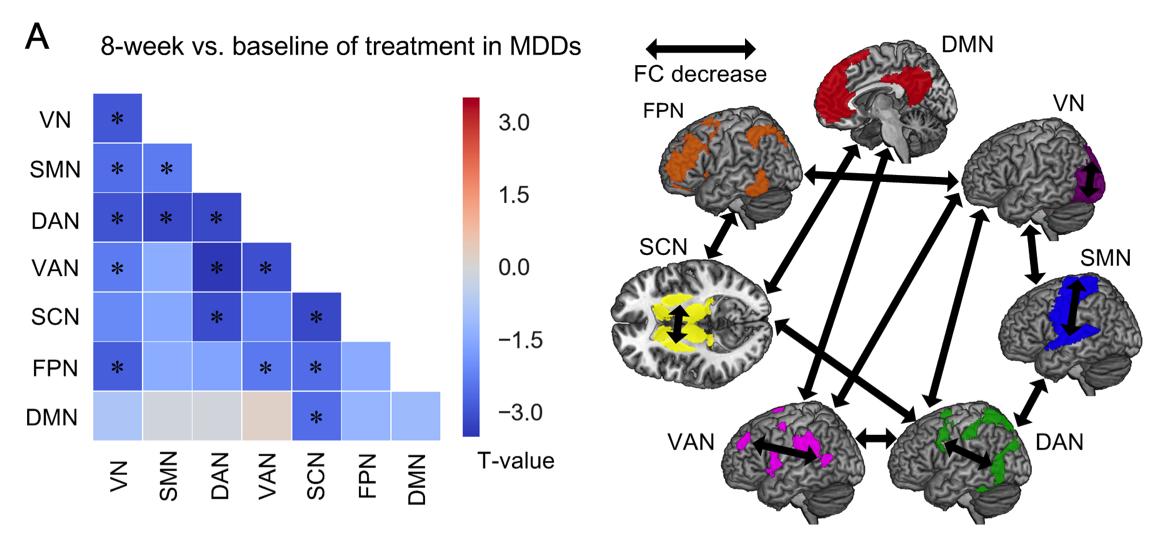
图11: 大规模网络分析显示药物治疗后大脑内广泛的功能连接减低
(2)新型药物氯胺酮
另外,最近还有一种新兴的药物叫做氯胺酮。以前它是一种俗称“k粉”的毒品,但是目前医学发现它对抑郁症有特别好特别快的疗效(Zarate, C. A. et al., 2006)。而传统抗抑郁药物的疗程较长,一般在前两周是没有正效果的,在两周之后才会慢慢起效。但氯胺酮服用之后,情绪立即就能得到改善。如果抑郁症患者有自杀的企图,氯胺酮能够快速的起到抑制作用,它还能够用于难治性抑郁。科学家们正在研究它在大脑中的作用机制,并如何去除它的毒品效应,让它成为一种更好的抗抑郁药物
3、物理治疗
最后,还有一部分患者,各种药物对他们都是不起效的,这种药物难治型的患者则要考虑其他物理治疗手段。
(1)电休克疗法
一种非常常见的物理治疗方法是电休克疗法(Electroconvulsive Therapy, ECT),这种方法通常需要将患者麻醉之后施加一个很大的电流,通过电击似乎对我们大脑起到了“重启”的效果,药物难治型患者通过这种物理治疗的方法也能获得很好的疗效。
(2)TMS治疗
我们实验室也在做经颅磁刺激(Transcranial Magnetic Stimulation, TMS)的研究。TMS治疗目前也作为一种治疗抑郁症的物理方法,是通过在大脑外面用一种高变的线圈产生高变的磁场,在脑内引起相应的电流变化来刺激大脑,改变大脑活动产生治疗抑郁的效果。而这种疗法的特点在于我们可以操纵机械臂使电流直接刺激大脑的特定区域,如同对我们的大脑进行“针灸治疗”,一个前沿方向是目前研究者正在寻找治疗抑郁症的具体“穴位”。
例如,正念疗法虽然可以加强核心子系统和背内侧前额叶子系统的功能连接,改善反刍思维从而降低我们的抑郁程度。但是正念治疗通常对于练习者有较高的要求,有的练习者很难沉下心来坚持做一些正念观的训练,并感到努力摆脱回忆的过程非常的痛苦。未来TMS治疗也许可以作为一种更为轻松的手段,通过经颅磁刺激,直接刺激大脑的相应通路来打破这种反复的循环来干预抑郁。

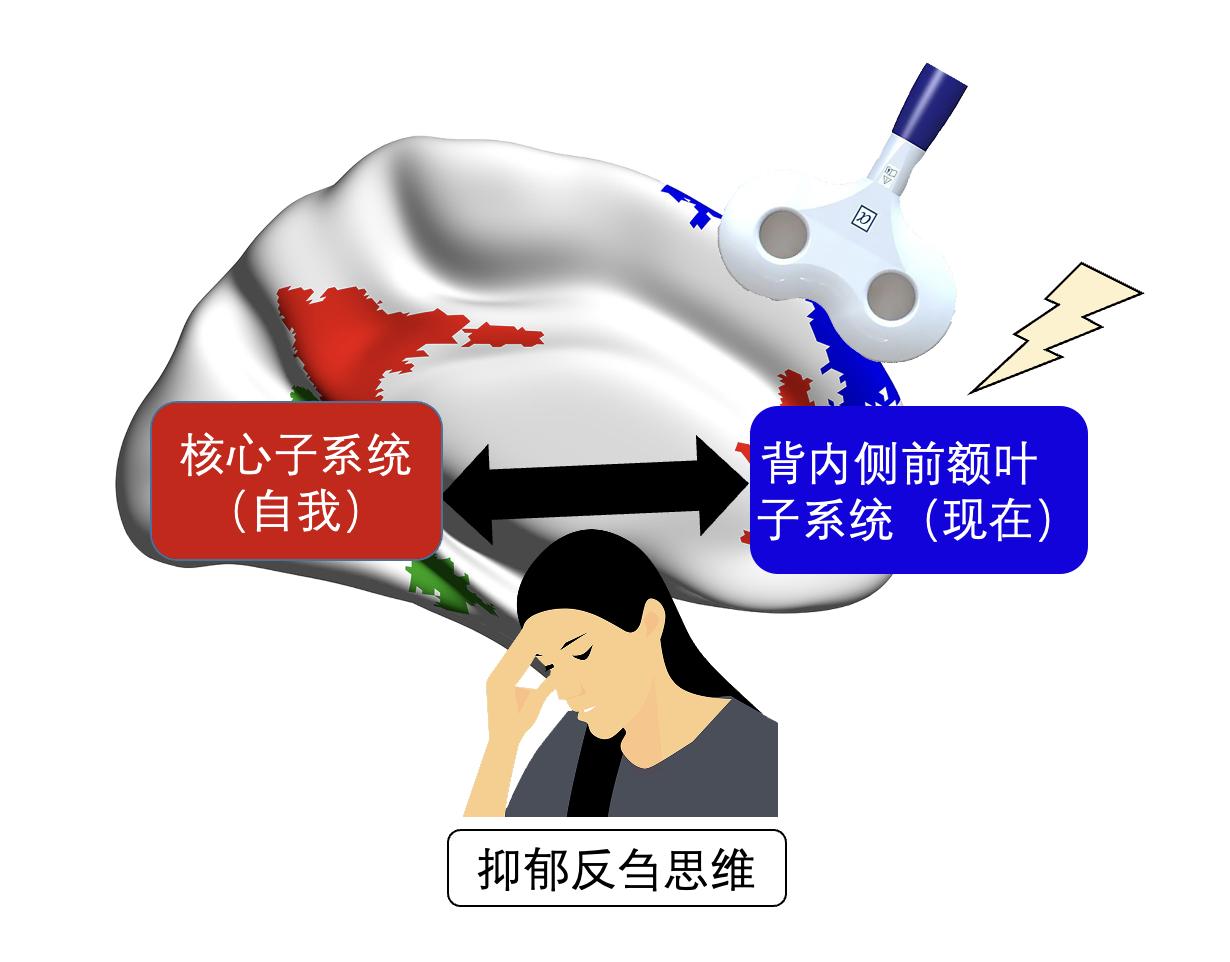
图12:找到大脑的个体化靶点进行精准的经颅磁刺激以提高疗效
4、综合疗法的发展以及利用脑科学方法为抑郁症进行分型诊断和确定治疗方式
我们希望在未来,可以通过大脑扫描(fMRI)知道患者是否真的患上了抑郁症,找到他们大脑异常的地方到底在哪里,再通过这种TMS机器人(图13)直接精准刺激他们大脑相应的靶点以达到更好的治疗效果;或是我们可以依据大脑扫描的结果为患者进行疾病的分型,不同类型的患者可以指导服用不同的药物;每个患者都是独特的,我们还可以根据每个患者大脑的特点,在心理治疗中选择干预不同的心理功能(如认知功能,奖赏功能,情绪功能……)。
如果我们能够读懂抑郁的大脑在想什么,确定抑郁症的病因,再选择对应最适合的治疗方式,目前肆虐全球的抑郁症也许就不再可怕。我们十分希望抑郁症的最新神经科学研究能够帮助到世界上的每一位抑郁症患者,能够对现在精神医学的诊断和治疗方式有所贡献。
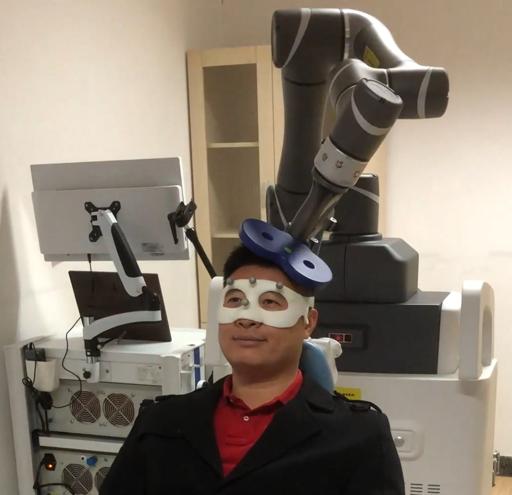
图13:TMS机器人直接刺激大脑靶点
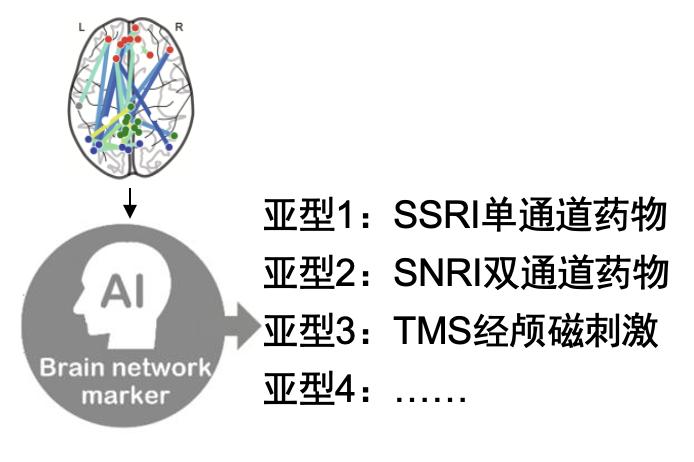
图14:利用脑影像数据为抑郁症进行分型诊断和对症治疗
参考文献:
Chen, X. , Chen, N. X. , Shen, Y. Q. , Li, H. X. , & Yan, C. G. . (2020). The subsystem mechanism of default mode network underlying rumination: a reproducible neuroimaging study. NeuroImage, 221, 117185.
Huang et al. (2019). Prevalence of mental disorders in china: a cross-sectional epidemiological study. The Lancet Psychiatry
Li, L. , Su, Y. A. , Wu, Y. K. , Castellanos, F. X. , & Yan, C. G. . (2021). Eight-week antidepressant treatment reduces functional connectivity in first-episode drug-nave patients with major depressive disorder. Human Brain Mapping(5).
Li, H.X., Lu, B., Chen, X.et al. (2022). Exploring self-generated thoughts in a resting state with natural language processing. Behavior Research Methods, 54(4):1725-1743.
Nolen-Hoeksema et al. (2008). Rethinking rumination. Perspectives on Psychological Science, 3, 400-424. doi:10.1111/j.1745-6924.2008.00088.x
Shen, Y. Q. , Zhou, H. X. , Chen, X. , Castellanos, F. X. , & Yan, C. G. . (2020). Meditation effect in changing functional integrations across large-scale brain networks: preliminary evidence from a meta-analysis of seed-based functional connectivity. Journal of Pacific Rim Psychology, 14.
Yan et al. (2017). Aberrant development of intrinsic brain activity in a rat model of caregiver maltreatment of offspring. Translational Psychiatry, 7(1), e1005.
Yan et al. (2019). Reduced default mode network functional connectivity in patients with recurrent major depressive disorder. Proceedings of the National Academy of Sciences of the United States of America, 116(18).
Zarate, C. A. , Singh, J. B. , Carlson, P. J. , Brutsche, N. E. , Ameli, R. , & Luckenbaugh, D. A. , et al. (2006). A randomized trial of an n-methyl-d-aspartate antagonist in treatment-resistant major depression. Archives of General Psychiatry, 63(8), 856-64.
Zhou, H. X. , Chen, X. , Shen, Y. Q. , Li, L. , & Yan, C. G. . (2019). Rumination and the default mode network: meta-analysis of brain imaging studies and implications for depression. NeuroImage, 206, 116287.